Los haluros de alquilo son alcanos con un haluro como uno de sus sustituyentes, estos presentan cierta polaridad ya que los halógenos son más electronegativos que los carbonos, por esa razón el carbono es parcialmente positivo y el haluro parcial negativo.
Esto le permite al carbono actuar como electrófilo, recibiendo electrones de un nucleófilo, preferiblemente fuerte, expulsando así al haluro, conocido como sustrato, ocurriendo de esta forma la sustitución nucleofílica, y de eso hablaremos en este post, sobre la SN2.
Sustitución nucleofílica bimolecular (SN2)
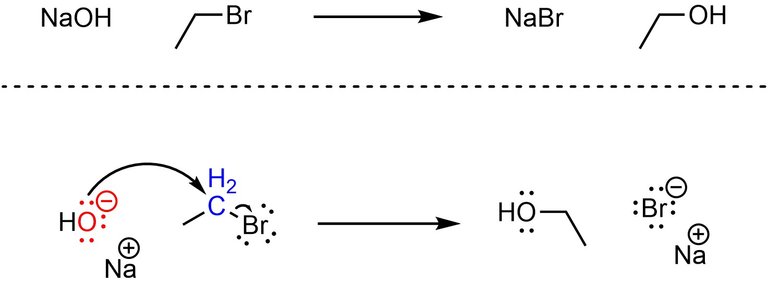
Para ello partiremos de la siguiente reacción
Aquí podemos observar una reacción entre bromuro de etilo e hidróxido de sodio, en ella el -OH actúa como base fuerte y ataca al carbono con carga parcial positiva, expulsando al grupo Br, esta reacción ocurre de forma inmediata, ya que cada reactivo es de primer orden y la reacción es de segundo orden global, dependiendo la velocidad de la reacción de ambos reactivos, de ahí el nombre de sustitución nucleofílica bimolecular.
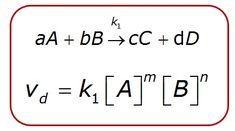
Ejemplo de reacción de segundo orden global, en estos casos al duplicar la cantidad de uno de los reactivos se duplica la velocidad de la reacción. Fuente de imagen
Factores que influyen en la reacción SN2
En este tipo de reacciones existen varios factores que influyen en la efectividad de la reacción, tales como:
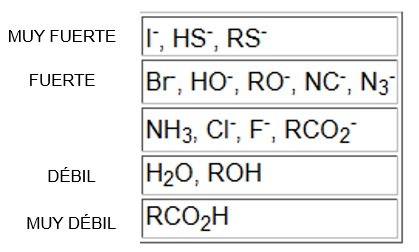
Fuerza del nucleófilo y su electronegatividad
Obviamente mientras más fuerte sea el nucleófilo más rápido atacará al carbono electrófilo, pero, ¿como identificamos a un buen nucleófilo? Sabemos que un nucleófilo tiene electrones para donar, podríamos suponer a partir de esa afirmación que un compuesto con carga negativa es un nucleófilo más fuerte que uno neutro, dicho de otro modo, una base es más nucleofílica que su ácido conjugado. Pero, ¿esto quiere decir que una base siempre será un nucleófilo? Esa sería una afirmación errónea ya que la definición de base es una sustancia que abstrae protones, y un nucleófilo ataca carbonos electrófilos, aunque en la mayoría de casos una base fuerte coincide con un nucleófilo fuerte.
También influye la electronegatividad del compuesto, mientras más electronegativo sea más unidos están los electrones no enlazados, disminuyendo la posibilidad de formar nuevos enlaces.
Impedimento estérico y efecto del disolvente
Para funcionar como un nucleófilo, un ion o molécula debe acercarse a un átomo de carbono para atacarlo. Los grupos voluminosos del nucleófilo dificultan este acercamiento y disminuyen la rapidez de reacción. El impedimento estérico influye poco en la basicidad, ya que la basicidad implica el ataque a un protón no impedido.
También cabe destacar la influencia que ejercen los disolventes sobre los nucleófilos. Entre estos disolventes están los disolventes próticos, los cuales contienen protones ácidos que forman enlaces por puentes de hidrógeno con los nucleófilos que tienen carga negativa, favoreciendo la solvatación de los aniones pequeños, mientras que los disolventes apróticos favorecen la nucleofilia de los aniones en general por tener una capacidad de solvatación débil, esto hace que los reactivos iónicos, más polares, sean insolubles en disolventes apróticos simples como los alcanos.
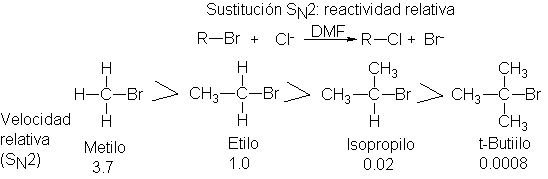
Reactividad del sustrato y estereoquimica de la reacción
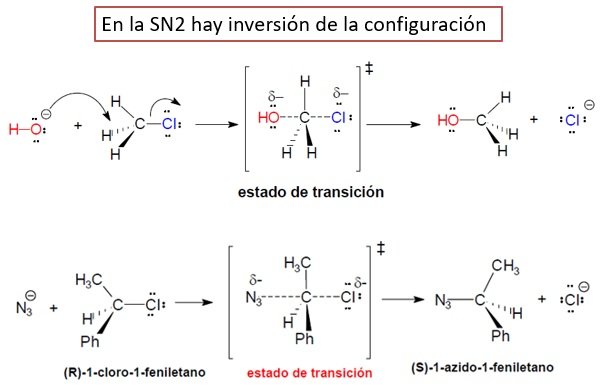
En este tipo de reacciones es importante que el sustrato sea un aceptor de protones para polarizar al carbono, sin eso la reacción no podría ocurrir, además de tener estabilidad luego de ser expulsado y polarizable para estabilizar el estado de transición y reducir la energía de activación. También influye en este tipo de reacciones el tamaño del sustrato, ya que si este es un haluro de metilo, es primario o secundario puede ocurrir la reacción, sin embargo esto no ocurre con los sustratos terciarios. Sobre la estereoquimica de esta reacción es necesario saber que el nucleófilo al realizar el ataque a la parte posterior invierte la configuración del carbono, asumiendo el nucleófilo una posición opuesta a la posición del grupo saliente original. Esto es un buen ejemplo de una reacción estereoespecífica, aquella en la que distintos estereoisómeros reaccionan para dar distintos estereoisómeros del producto.
Espero les haya gustado y que dejen su apoyo para más contenido de química.
- Basado en el Wade Leroy G. Química Orgánica.