Autor: @madridbg, a través de Power Point 2010, utilizando imágenes de dominio público. Rajesh Balouria
Saludos y bienvenidos estimados lectores de esta apasionante plataforma, el día de hoy estaremos socializando a través de las comunidades @stemsocial, @stem-espanol y @cervantes contenidos de carácter científico asociado con la importancia que presenta el átomo de carbono para la disciplina o rama de la química a quien denominamos orgánica.
En este sentido, centraremos nuestra atención en los tipos de enlaces que este elemento forma y que le permite convertirse en uno de los elementos fundamentales para el desarrollo de la vida y la industrialización en general.
INTRODUCCIÓN

Desde que el hombre inicio con el proceso de transformación de la materia, que parte como una relación directa al descubrimientos del fuego, se lograr determinar la capacidad investigativa de la especie y se da inicio a una seria de escenario que nos permite comprender el funcionamiento de la materia, así como la utilidad que podemos extraer de esta.
En este sentido, uno de los aspectos que más intriga al hombre es la diferencia que presentaba las sustancias que constituían a las especies vivas de aquellas que presentaban lo minerales, aspectos que se empezó a investigar a partir del siglo XVIII, donde las investigaciones en el campo experimental logra detectar que la materia orgánica presenta puntos de fusión más bajos y un proceso de descomposición más acelerado cuando se sometían al calor, de igual forma la manipulación y purificación de estas sustancias era más difícil, de modo que para diferenciar los aspectos encontrados, decidieron enunciar lo que hoy se conoce como química orgánica.

Fig. 2. Representación de Wöhler y el estudio de la síntesis de la urea. Autor: Bensaccount
De allí que esta rama de la química, se centra en el estudio exclusivo de la materia orgánica responsable de la vida, en especial de las propiedades y utilidad del carbono, por lo cual, esta disciplina también se le conoce como la química del carbono.
Partiendo de lo anterior, es válido realizarnos los siguientes planteamientos:
¿Qué tiene el carbono de especial y por qué todavía se considera la química orgánica como una rama especial de la ciencia?

La respuesta a estos planteamiento es si se quiere algo simple, ya que responden a la capacidad que tiene este átomo para unirse con elementos igual o diferentes a él, lo cual le permite formar grades cadenas lineales y abiertas o en su defectos compuestos cíclicos.
Partiendo de lo anterior, este elemento es capaz de generar múltiples compuestos químicos y estar presente tanto en compuesto orgánicos como inorgánicos, donde la cantidad en masa del átomo es variables y puede encontrarse desde el metano con 1 átomo de carbono, hasta el ácido desoxirribonucleico (ADN), con decenas de miles de millones de átomos de carbono.
En la actualidad se registran más de 30 millones de compuestos orgánicos asociado con el carbono y con las investigaciones diarias terminan obteniéndose nuevos compuestos que sirven de sustento para la exigencia de la sociedad.
NATURALEZA DE LA MATERIA ORGÁNICA, PROPIEDADES DE ENLACE DEL CARBONO

Como bien se expresa en el título de este apartado, haremos un recorrido por las principales características que permiten comprender la capacidad de enlace del carbono, entre estas destacan:
1. Organización espacial del átomo de carbono: en general las moléculas orgánicas exhiben una estructura tridimensional, debido a la repulsión que se genera entre sus átomos a causa de los electrones de valencia. En este sentido, si el carbono se une a cuatro elementos, se obtiene una molécula tetraédrica donde los vértices adquieren un ángulo de 109.5°, tal como se presenta en el caso de metano (CH4).
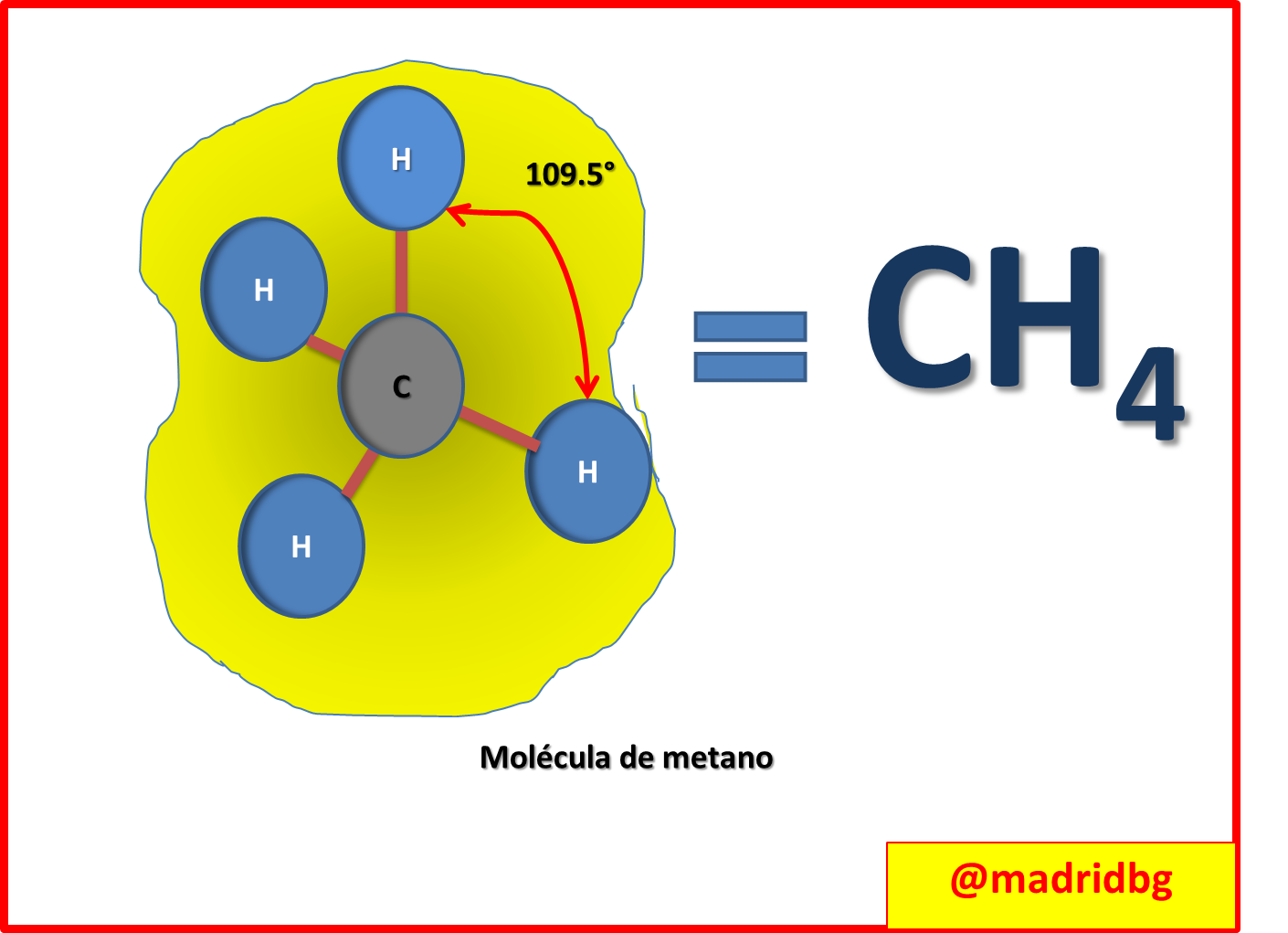
Fig. 3. Representación de la molécula de metano. Autor: @madridbg, a través de Power Point 2010.
2. Electrones de valencia: como este elemento se caracteriza por presentar cuatro electrones de valencia, de acuerdo a la hibridación (1s2 2s2 2p2), propiedad que le proporciona la capacidad de enlace antes mencionada.
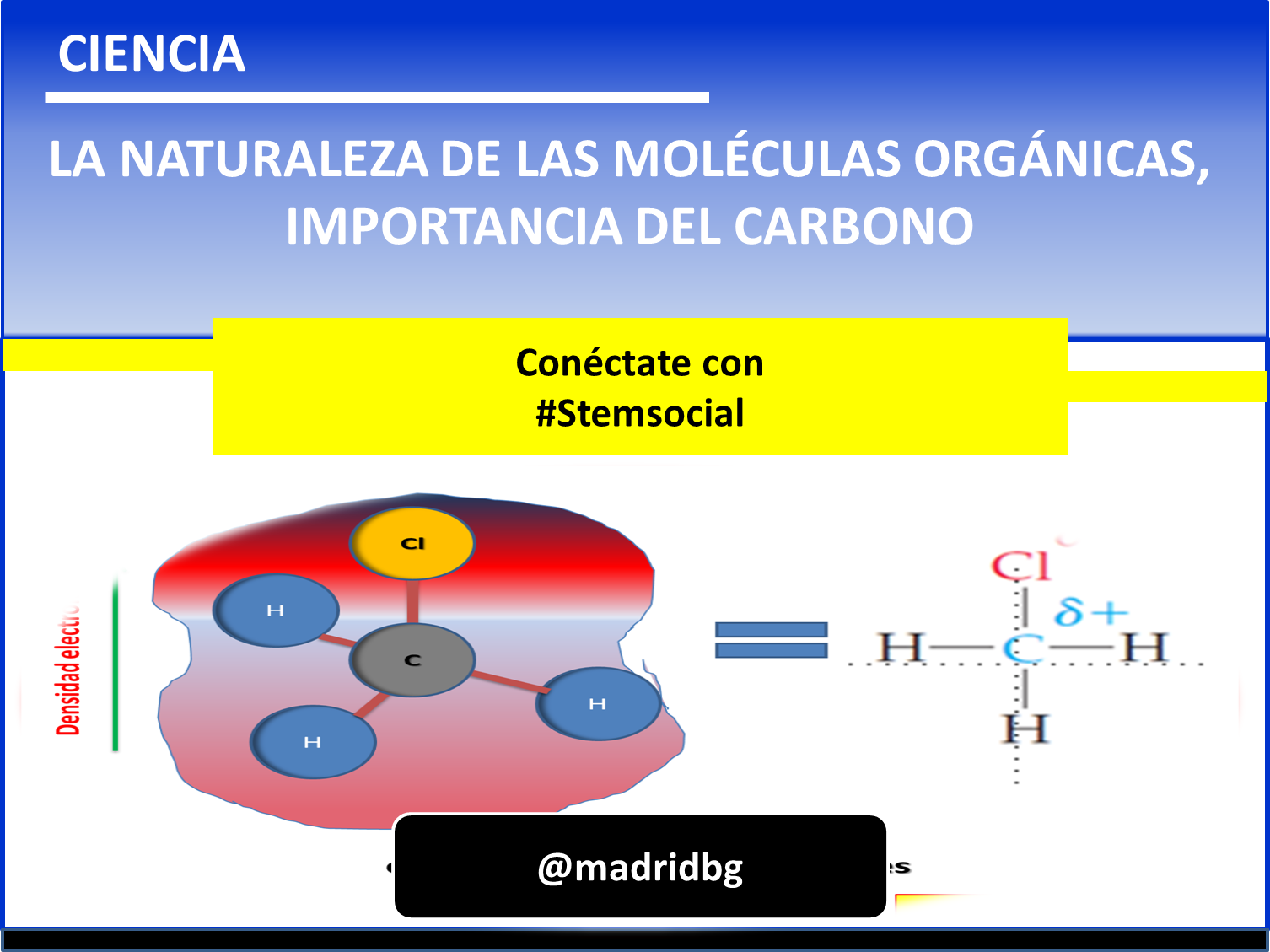
3. Enlaces covalentes polares: recordemos que esta propiedad está estrechamente relacionada con la electronegatividad de los elementos, en este sentido, si el átomo se carbono se une con elementos del lado derecho de la tabla periódica, por ejemplo el cloro para formar el cloro metano. Se produce una atracción de la densidad electrónica del elemento más electronegativo sobre el menos electronegativo, formando un enlace covalente con características polares debido a la fuerte atracción electrónica que ejerce el cloro sobre el átomo de carbono.

Fig. 4. Representación de la molécula de cloro metano y su densidad electrónica. Autor: @madridbg, a través de Power Point 2010.
4. Enlaces covalentes múltiples: el átomo de carbono puede generar este tipo de enlaces ya que puede compartir dos o más electrones con los átomos adyacentes, tal es el caso del etileno donde podemos observar que el carbono compartes 4 electrones con su átomos vecino.

Fig 5. Representación de la molécula de etileno. Autor: @madridbg, a través de Power Point 2010.
En función de lo anterior, es preciso establecer que son los enlaces covalentes los que mantienen unidas las estructuras orgánicas, de allí que este tipo de elemento presenten punto de fusión y ebullición menores a las sustancias iónica y este comportamiento, hace que gran parte de los compuestos orgánicos simples sean líquidos a temperatura ambiente e insolubles en agua.
CONSIDERACIONES FINALES

Sin duda conocer las características y propiedades de las familia de los compuesto nos permite generar una visión más amplia acerca del comportamiento de estas sustancias químicas, en el caso del átomo de carbono, por ser un átomo indispensables para muchos proceso de nuestra existencia, adquiere un mayor valor, de allí que la química orgánica se ha centrado en el estudio y comprensión del átomo en particular.
En líneas generales podemos afirmar que el átomo de carbono cumple funciones diversas pero una de las mayores cualidades es que se comporta como pequeños bloques de construcción que mantiene unidad la materia orgánica.
BIBLIOGRAFÍA CONSULTADA

[1] McMURRY E., John y Fay C., Robert. (2008). Química general. Quinta edición PEARSON EDUCACIÓN, México, 2009 ISBN: 978-970-26 1286-5.
[2] Ralph, H. Petrucci, William S. Harwood, E. Geoffrey Herring. (2003). QUIMICA GENERAL. Octava edición. PEARSON EDUCACIÓN. S.A., Madrid.
DE INTERÉS

1. La imagen de portada fue realizada por @madridbg, utilizado imagen de dominio publico
2. Para más información relacionada con las áreas de ciencia, tecnología, ingeniería y matemáticas, no dudes en visitar #stemsocial y #stem-espanol, son comunidades que promueven avances científicos en estas áreas

#posh twitter:
The rewards earned on this comment will go directly to the person sharing the post on Twitter as long as they are registered with @poshtoken. Sign up at https://hiveposh.com.
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider delegating to the @stemsocial account (85% of the curation rewards are returned).
You may also include @stemsocial as a beneficiary of the rewards of this post to get a stronger support.