
Autor: @madridbg, a través de Power Point 2010, utilizando imágenes de dominio público.
Bienvenido nuevamente estimados miembros de la plataforma #hive y en especial aquellos usuarios que hacen vida a diario en las comunidades de habla hispana con mayor aporte académico asociado al área de las ciencia #stemsocial, #stem-espanol y #cervantes. En esta oportunidad, abordaremos a profundidad aquellos apartados conceptuales que pudieron quedar en el aire, al momento de dictar el conversatorio para la comunidad de #stem-espanol, actividad que impulsan cada semana los compañeros @carloserp-2000 y @iamphysical.
Sin duda, “el conversatorio” es un espacio dinámico y nutritivo en lo que a conocimiento se refiere, allí se abordan las diferentes perspectivas del conocimientos, enfocado desde la formación académica de los que hacemos vida en el mismo. Por los cual, me atrevo a definirlo como un espacio interdisciplinar, donde convergen diferentes áreas y disciplinadas de estudio.
INTRODUCCIÓN
Al hablar de quiralidad, es necesario establecer patrones de comparación que permiten comprender el fenómeno que se estudia. En este sentido, la mejor forma de entender la organización espacial de los compuestos orgánicos es a través del comportamiento de nuestra mano izquierda sobre la derecha y viceversa. Si analizamos las mismas, podemos observar que una es la imagen especular no superponible de la otra, es decir, una imagen es el reflejo de la otra como si la estuvieras viendo a través de un espejo, comportamiento que se conoce como quiralidad .
Este comportamiento, también se presenta en los compuestos orgánicos donde el arreglo espacial que adoptan las moléculas influirá en la actividad biológica o farmacológica de la sustancias. Por consiguiente, el comportamiento fármaco-dinámico y fármaco-cinético de los compuesto orgánicos asociados a los medicamentos esta influenciados por las características quirales del mismo.
A sabiendas que en la actualidad, la mayoría de los fármacos que salen al mercado presentan un comportamiento óptico frente a la luz polarizada (son quirales) y donde su función está determinada por el giro que pueda presentar la molécula de estudio. De tal modo, en esta publicación, estaremos abordando la fundamentación química y el comportamiento que asumen los enantiómeros, diasteroisómeros, mezclas racémicas, en otros, presente en los medicamentos.
ESTRUCTURA DEL CARBONO FRENTE A LA ACTIVIDAD ÓPTICA
Químicamente el átomo de carbono es considerado como un elemento tetraédrico, lo cual le da la capacidad de formar enlaces con el mismo y con otros elementos, por tal sentido, está presente en un gran número de compuestos que conocemos y que forma parte de toda la materia orgánica del planeta, de allí radica su importancia y atención por parte de la química orgánica.
De igual forma, es un elemento que tiene la capacidad de formar cuatro enlaces simultáneos con radicales similares o diferentes entre sí. A nivel de la isomería óptica, cuando el carbono se une a cuatros sustituyentes diferentes sin un plano de simetría en la molécula, da como resultados la formación de enantiómeros cuyos compuestos son de interés practico a nivel de la industria farmacológica y los cuales son concebido como sustancias que tienen una imagen especular no superponibles, concepto que abordamos en el apartado previo.
Imagen 2. Quiralidad en los átomos de carbono. Autor: @madridbg, a través de Power Point 2010.
En este punto de la temática resulta necesario recordar, que la actividad óptica está limitada por dos condiciones que permiten la quiralidad dentro de las moléculas. La primera, hace referencia a la presencia de un átomo quiral (átomo con cuatro sustituyentes diferentes) y la segunda, que no exista un plano de simetría en la molécula como se observa en la imagen siguiente.
Imagen 3. Formas para predecir la quiralidad en las moléculas. Autor: @madridbg, a través de Power Point 2010.
A diferencia de los enantiómeros que se forma con la presencia de un átomo quiral, los diateroisómeros, son el resultado de una molécula con dos o más centros quirales lo que origina diferentes compuestos que presentan el mismo tipo y cantidad de átomos, las mismas propiedades físicas y química pero difieren en su comportamiento biológico y farmacológico.
De igual forma, en aquellas moléculas donde existen 2 o más centros quirales pueden aparecer sustancias denominadas compuesto meso y se producen a causa de una simetría interna en la molécula, los cual al girar 180° termina formando el mismo compuesto y no se generan los diateroisómeros esperados.
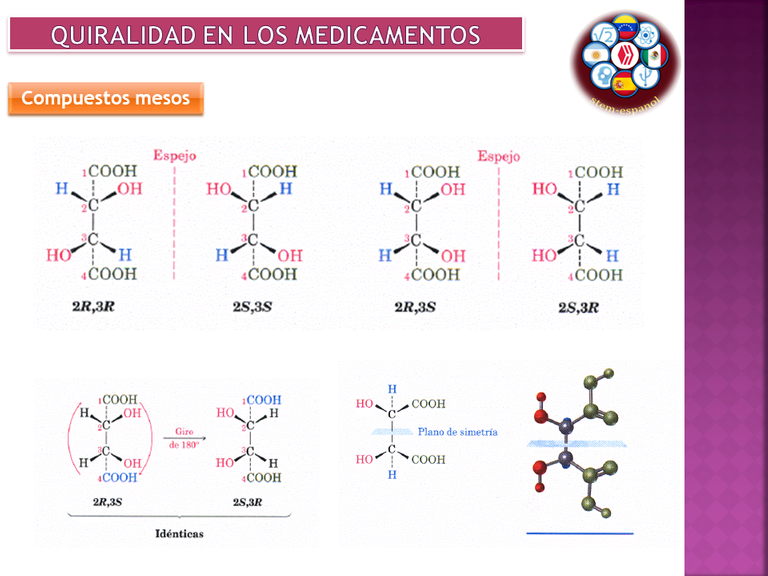
Imagen 4. Simetría interna en los compuestos meso. Autor: @madridbg, a través de Power Point 2010.
Por su parte las mezclas racémicas, otro tipo de sustancia que se genera a causa de la quiralidad, se refieren a que en la misma molécula existen tanto el enantiómeros como su imagen especular en concentraciones 50-50, por lo que la actividad óptica se anula entre ellos. Este tipo de molécula, junto a los enantiómeros son las más estudiadas por la industria farmacológica debido a los diferentes comportamientos fármaco-cinéticos y fármaco-dinámicos de los mismos.
Imagen 5. Las mezclas racémicas y la actividad óptica. Autor: @madridbg, a través de Power Point 2010.
EL POLARÍMETRO EN LA DETECCIÓN DE LA ACTIVIDAD ÓPTICA
En publicaciones anteriores, abordamos lo concernientes a las radiaciones electromagnéticas. En este sentido, es oportuno recordar que la luz ordinaria viaja en diferentes direcciones de tal manera que se convierte en polarizada cuando se logra concentrar en un solo plano, función que cumple el polarímetro. Una vez polarizada la luz, se hace coincidir con la muestra de la sustancia objeto de estudio para determinar el giro que provoca en la luz polarizada.
A través del comportamiento de la luz, se puede establecer si las sustancias son dextrórrotatorias (gira el plano de la luz hacia la derecha) o levórrotatorias (gira el plano de la luz hacia la izquierda), lo cual permite vislumbrar la presencia de la actividad óptica en la molécula química que se está estudiando.
Este comportamiento, fue señalado por Jean Baptist Biot, científico francés que estudiaba la naturaleza de la luz en un plano y quien realizó las primeras observaciones acerca del comportamiento de ciertas moléculas químicas frente a la luz polarizada.
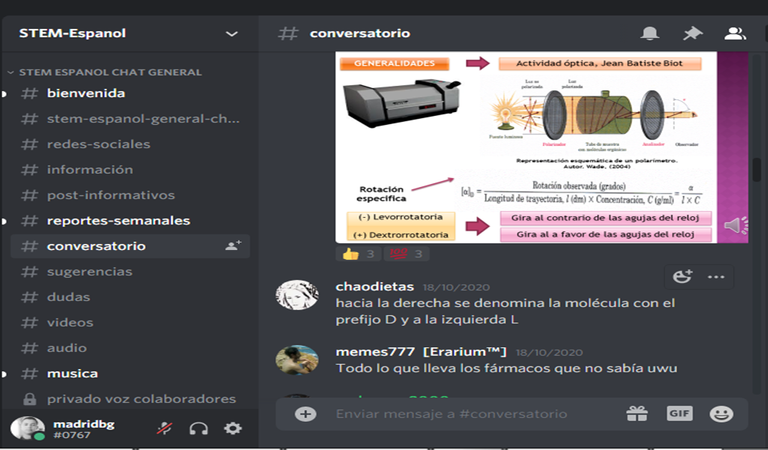
Imagen 6. Funcionamiento del polarímetro. Autor: @madridbg, a través de Power Point 2010. Usando aportes de Wade. (2011)
CONFIGURACIÓN ESPACIAL DE LOS ÁTOMOS Y LA QUIRALIDAD
Como se mencionó en el apartado anterior, el polarímetro nos permite determinar si la molécula es dextrógira o levógira, pero no podemos determinar a través de este, la configuración o el arreglo espacial que adoptan los diferentes átomos que están presentes en la molécula química. Por consiguiente, tras las investigaciones realizadas por Cahn-Ingold-Prelog, se puede establecer una secuencia de pasos o reglas para predecir el comportamiento espacial de las sustancias.
Los mismos los resumiremos a continuación:
Paso 1: Utilizar como patrón de referencia el numero atómico de los átomos presentes en cada sustituyente unido al átomo quiral y establecer jerarquía de acuerdo a la molécula de mayor tamaño.
Paso 2: Si no es posible establecer un orden entre las moléculas utilizando el primer átomo, hay que avanzar al siguiente hasta conseguir la primera diferencia.
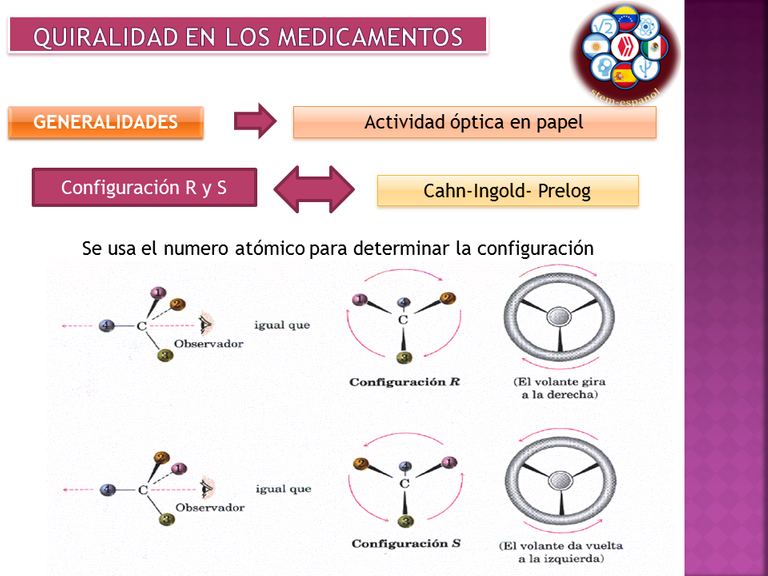
Imagen 7. Configuración R y S y la actividad óptica. Autor: @madridbg, a través de Power Point 2010. Usando aportes de Wade. (2011)
Una vez marcada las prioridades de cada sustituyente se traza una línea en la trayectoria de los mismos, la cual no permitirá establecer la configuración espacial de la sustancia, bajo la configuración (R y S) de acuerdo al giro que se presente.
R = el giro se produce a la derecha o siguiendo las agujas del reloj.
S= el giro se produce a la izquierda o al contrario de las agujas del reloj.
QUIRALIDAD EN LOS MEDICAMENTOS: COMPORTAMIENTO DUAL DE LAS SUSTANCIAS QUIMICAS.
A nivel industrial los principios activos usados en la elaboración de medicamentos provienen de la naturaleza y otros por síntesis o modificaciones químicas a nivel de laboratorio. Estas últimas, son las que más problemas general a nivel farmacológico ya que se pueden presentar en forma de mezclas racémicas y no como enantiómeros puros.
Por consiguiente, en este apartado describiremos algunas desventajas e inconveniente de los usos de medicamentos racémicos en vez de los enantiómeros puros. Recordemos que una mezcla racémicas es una combinación 50-50 del enantiómero y su imagen especular, es decir, el 50% es levógiro y el otro 50% es dextrógiro, por lo que a pesar de tener las mismas propiedades su comportamientos biológico y farmacológico son diferentes ya que la organización espacial de los átomos es diferentes.
Imagen 8. Especificidad de las moléculas quirales. Autor: @madridbg, a través de Power Point 2010. Usando aportes de Chang. (2010)
La razón de su comportamiento se debe a la interacción entre el fármaco y los sitios activos del sustrato, los cuales como lo podemos observar en la imagen anterior, estas sustancias presentan una especificidad como una cerradura con su llave y se rigen con el mismo principios del funcionamiento enzimático, por lo que la fármaco-dinámica y la fármaco-cinética se hacen más complejas en las mezclas racémicas ya que se deben estudiar cada enantiómeros por separado.
Un ejemplo lamentable de este comportamiento es el suscitado con el fármaco talidomida, un medicamento en forma de mezcla racémicas, que era recetados como sedante y como calmante de las náuseas en mujeres embarazas, en cierta medida el medicamente bajo su configuración (R) cumplía con el objetivo farmacológico estipulado. Para sorpresa de muchos la configuración (S) ocasionaba estragos en el feto de las mujeres que lo consumían. Donde se detectaron efectos teratogénicos marcados en los niños al nacer, presentando malformaciones a nivel de miembros superiores e inferiores.
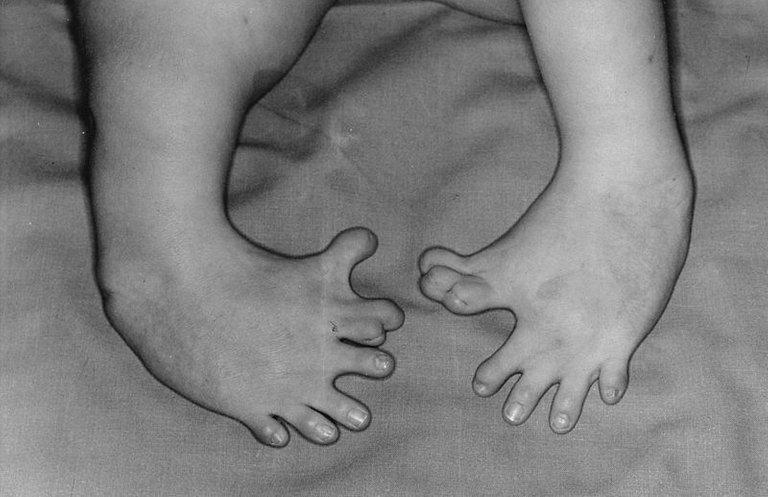
Imagen 9. Daños colaterales de la talidomida. Extraido de: Otis Historical Archives National Museum of Health and Medicine.
De allí, radica la importancia de dar a conocer esta información y donde a nivel farmacológico se hacen estudios a diarios que permitan generan fármacos basados en enantiómeros puros ya que estos son más eficiente y eficaces al momentos de tratar una patología.
APORTES DE LA TEMÁTICA
El aporte de la temática la abordare desde dos puntos de vista, el primero hace referencia a mi participación en el conversatorio, el cual permitió trasmitir mis conocimientos en el área de la química con personas de diferentes contexto académicos donde se pudo evidenciar lo refrescante y nutritivo de este tipo de actividades. En segundo lugar, a través de la publicación se pudo reforzar lo concerniente a la quiralidad y evaluar la importancia de generar los estudios químicos necesarios a los medicamentes antes de sacarlos al mercado, de modo que no se presenten más casos como el de la talidomida.
BIBLIOGRAFÍA CONSULTADA
[1] Chang, R. (2010). Química. Decima edicion. McGraw-hill Interamericana editores. ISBN: 978-607-15-0307-7.
[2] Juaristi Eusebio. (2005). ). Izquierda y derecha en química: la quiralidad. Ciencia Artículo: Acceso en línea .
[3] McMURRY E., John y Fay C., Robert. (2008). Química general. Quinta edición PEARSON EDUCACIÓN, México, 2009 ISBN: 978-970-26 1286-5.
[4] Ralph, H. Petrucci, William S. Harwood, E. Geoffrey Herring. (2003). QUIMICA GENERAL. Octava edición. PEARSON EDUCACIÓN. S.A., Madrid.
[5] Vaquero Juan José. Metodologías químicas en el descubrimiento de nuevos fármacos. Universidades de Alcalá, Complutense y S. Pablo-CEU Doctorado Interuniversitario QUIMICA MEDICA Artículo: Acceso en línea .
[6] WADE, LEROY. (2011). . QUÍMICA ORGÁNICA. VOLUMEN 2. SÉPTIMA EDICIÓN. PEARSON EDUCACIÓN. MÉXICO. ISBN: 978-607-32. ÁREA: CIENCIAS
DE INTERÉS
Para más información relacionada con las áreas de ciencia, tecnología, ingeniería y matemáticas, no dudes en visitar #stemsocial y #stem-espanol, son comunidades que promueven avances científicos en estas áreas

Has sido votado por
PROYECTO ENLACE
'Conectando Ideas y Comunidades'
PROYECTO ENLACE es un proyecto de curación de habla hispana enfocado en recompensar contenido de calidad y apoyar autores en su proceso de crecimiento en HIVE.
Creemos y apostamos por el futuro de esta gran plataforma, y estamos muy emocionados de poder hacerla crecer junto a esta comunidad. Así que te invitamos a usar nuestra etiqueta ENLACE y estar atento a todas las actividades que tenemos preparadas y que estaremos publicando en breve.
Atentamente
EQUIPO ENLACE 2020
Gracias al equipo de enlace 2020 por la valoración positiva de la publicación.
Saludos @madridbg. Excelente actividad la del conversatorio, lástima que no se me ha hecho posible participar últimamente. Ciertamente la quiralidad es una propiedad muy estudiada en química, y los medicamentos ópticamente activos tienen claras ventajas sobre las mezclas racémicas, lo que conduce a una mejor efectividad.
Saludos mi estimado @emiliomoron, pues ultimamente son muchos los inconvenientes que se nos están presentando, aquí en el país Venezuela cuando no es el servicio eléctrico es el Internet el que nos limita la posibilidad de estar en esta actividad tan amena, donde nos nutrimos en conocimiento desde el abordaje de diferentes perspectiva. Nos seguimos leyendo.
Fantástico contenido estimado @madridbg fue un conversatorio maravilloso, gracias por tu valioso aporte
Saludos mi estimado @carloserp-2000, agradecido por el espacio que desde @stem-espanol nos brindan la posibilidad de desarrolla una actividad tan amena como lo es el conservatorio.